Study on the Vegetative Detritus Contribution to Beijing Urban PM2.5 Using Cellulose as a Marker
-
摘要: 大气细粒子(PM2.5)污染是全球尤其是我国许多城市的重要环境问题。利用示踪物质识别和估算大气颗粒物来源是公认的可靠技术,纤维素可以作为示踪物质表征一次颗粒物的天然植被排放来源。本文针对大气细粒子中纤维素含量低、全程序空白相对较高等难点,优化建立了纤维素酶水解、GOD-苯酚-四氨基安替比林测糖法,在我国首次应用于测定大气PM2.5中纤维素的含量,估算天然植被排放源的贡献。方法检出限为0.26 μg/m3(纤维素),可以满足大气PM2.5纤维素测定要求;而且有效地降低了空白,全程序空白值(36.5 μg葡萄糖)低于文献方法空白值(53.8 μg葡萄糖),使之更适合于PM2.5的测定。使用本方法对2012年5月至6月采集的北京市大气PM2.5样品进行分析,纤维素检出率为96%,纤维素的平均含量为(0.573±0.17) μg/m3,折合为天然植被排放量占PM2.5质量浓度的1.37%±0.65%;天然植被排放源对有机碳的平均贡献率为4.4%,最大达到9.2%,反映出天然植被排放是北京市PM2.5的重要来源之一。本研究方法为我国城市大气颗粒物(包括总悬浮颗粒物、PM10、PM2.5等)来源识别提供了新的手段。
-
关键词:
- 大气颗粒物PM2.5 /
- 示踪化合物 /
- 纤维素测定 /
- 天然植被排放
Abstract: PM2.5 pollution raises environmental concern in China and other countries worldwide. The marker technique is regarded as a reliable tool for atmospheric aerosol source tracing. Cellulose can be used as a marker to identify and evaluate vegetative detritus emission to primary aerosols. An analytical method for cellulose in the PM2.5 has been modified because of its low content in PM2.5 and the relative high procedure blank. The method combines an enzymatic cellulose hydrolysis procedure and a GOD-phenol-4-aminoantipyrene determination of formed glucose. The key parameters of the method were optimized as a delignification condition, temperature for cellulose enzymatic hydrolysis, amount of enzyme, pH value and hydrolysis reaction time. The method meets the requirements of cellulose determination of PM2.5 with a detection limit of 0.26 μg/m3. A procedure blank of 36.5 μg glucose was obtained which is significantly lower than 53.8 μg for the previous method. Cellulose in 23 Beijing urban PM2.5 collected from May 15th to June 28th, 2012 were analyzed. The detection rate of cellulose is 96%. The results show that the cellulose concentration in Beijing PM2.5 is (0.573±0.17) μg/m3. The vegetative detritus contribution is 1.37%±0.65% of PM2.5 mass concentration, or 4.4% in average and 9.2% in the maximum of PM2.5 organic carbon, indicating vegetative detritus is a major contributor of urban aerosol organic carbon and has to be considered in source attribution studies. This method provides a new technique for urban atmospheric PM2.5 source identification.-
Key words:
- atmospheric PM2.5 /
- marker /
- cellulose determination /
- vegetative detritus emission
-
-
表 1 PM2.5样品在不同温度下去木质素实验结果
Table 1. Delignification efficiency for PM2.5 samples at different temperatures
温度 纤维素含量平均值
m/μg(n=6)相对标准偏差
RSD/%70℃ 100.880 11.5 室温(25℃) 97.910 8.8 表 2 反应温度、pH值、纤维素酶加入量和反应时间对酶解反应产率的影响
Table 2. Effects of temperature,pH value,amount of celluclast and reaction time on enzymatic hydrolysis productivity
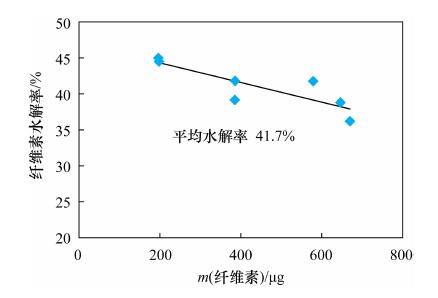
反应温度 水解率/% 40℃ 37.7±2.1 45℃ 39.9±4.2 50℃ 41.7±3.4 55℃ 23.2±1.7 反应pH值 水解率/% 4.5 41.7±4.0 5.0 36.3±3.2 5.5 22.2±4.8 纤维素酶用量 水解率/% 100 μL酶使用液
(原液稀释10倍)39.3±3.3 200 μL酶使用液 41.7±4.1 500 μL酶使用液 43.4±2.7 100 μL酶原液 47.2±7.2 200 μL酶原液 53.2±5.5 酶解反应时间 水解率/% 24 h 41.7±5.6 48 h 45.4±6.2 72 h 48.8±6.5 96 h 51.3±4.8 表 3 方法全程序空白、检出限和重现性
Table 3. Procedure blank,detection limit and reproducibility of the method
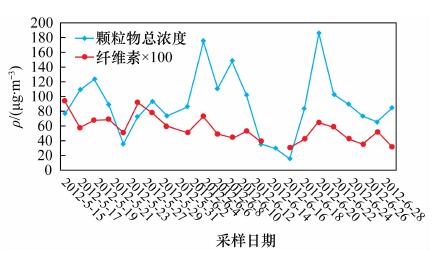
表 4 2012年5月~6月北京市大气PM2.5纤维素测定结果及与文献值的比较
Table 4. Cellulose in PM2.5 collected on May to June,2012 in Beijing and comparison with literatures
研究地点样品粒径
/μm采样时段 纤维素含量ρ/
(μg·m-3)天然植被
排放对颗粒
物质量浓度
贡献/%天然植被排放
对有机碳
贡献/%Vienna,Austria < 1.6 1994~1995 0.039 1.6 - Azores,Portugal < 2.5 2002~2004 0.032 - 4.6 Sonnblick,Astria < 2.5 2002~2004 0.046 - 7.8 本研究 < 2.5 2012 0.57 1.4 4.4 -
[1] 董凤鸣,莫运政,李国星,胥美美,潘小川.大气颗粒物(PM10/PM2.5)与人群循环系统疾病死亡关系的病例交叉研究[J].北京大学学报(医学版).网络出版地址: http://www.cnki.net/kcms/detail/11.4691.R.20130530.0849.001.html [2013-05-30].
[2] 谭吉华,赵金平,段菁春,马永亮,贺克斌,杨复沫.广州秋季灰霾污染过程大气颗粒物有机酸的污染特征[J].环境科学, 2013, 34 (5): 1982-1987. http://www.cnki.com.cn/Article/CJFDTOTAL-HJKZ201305048.htm
[3] 唐傲寒,赵婧娴,韩文轩,刘学军.北京地区灰霾化学特性研究进展[J].中国农业大学学报,2013, 18(3):185-191. http://www.cnki.com.cn/Article/CJFDTOTAL-NYDX201303028.htm
[4] He K, Yang F, Ma Y, Zhang Q, Yao X, Chan C K, Cadle S, Chan T, Mulawa P. The characteristics of PM2.5 in Beijing, China [J]. Atmospheric Environment, 2001, 35: 4959-4970. doi: 10.1016/S1352-2310(01)00301-6
[5] Zappoli S, Andracchio A, Fuzzi S, Facchini M C, Gelencser A, Kiss G, Krivacsy Z, Molnar A, Meszaros E, Hansson H C, Rosman K, Zebuhr Y. Inorganic, organic and macromolecular components of fine aerosol in different areas of Europe in relation to their water solubility [J].Atmospheric Environment,1999,33: 2733-2743. doi: 10.1016/S1352-2310(98)00362-8
[6] Matthias-Maser S, Jaenicke R. The size distribution of primary biological aerosol particles with radii >0.2 mm in an urban/rural influenced region [J]. Atmospheric Research, 1995, 39: 279-286. doi: 10.1016/0169-8095(95)00017-8
[7] Andreae M O.Biomass Burning: Its History, Use and Distribution and Its Impact on Environmental Quality and Global Climate [M]//Levine J S.Global Biomass Burning: Atmospheric, Climatic and Biospheric Implications. Cambridge: MIT Press, 1991: 3-21.
[8] Sicre M A, Marty J C, Saliot A.Aliphatic and aromatic hydrocarbons in different sized aerosols over the Mediterranean Sea: Occurrence and origin [J].Atmospheric Environment, 1987, 21(10): 22-47.
[9] 何凌燕,胡敏,黄晓锋,张远航.北京大气气溶胶PM2.5中的有机示踪化合物[J].环境科学学报,2005,25 (1): 23-29.
[10] Pacini E.Anther and pollen ripening to pollen presentation [J].Plant Systematics and Evolution, 2000, 222: 19-43. doi: 10.1007/BF00984094
[11] Lewis D, Smith D.Sugar alcohols (polyols) in fungi and green plants. Ⅰ: Distribution, physiology and metabolism [J]. New Phytologist, 1967, 66: 143-184. doi: 10.1111/nph.1967.66.issue-2
[12] Claeys M, Graham B, Vas G. Formation of secondary organic aerosols through photooxidation of isoprene [J]. Science, 2004, 303: 1173-1176. doi: 10.1126/science.1092805
[13] Rogge W F, Hildemann L M, Mazurek M A, Cass G R, Simoneit B R T. Sources of fine organic aerosol. 4. Particulate abrasion products from leaf surfaces of plants [J]. Environmental Science and Technology, 1993, 27: 2700-2711. doi: 10.1021/es00049a008
[14] Puxbaum H, Tenze-Kunit M. Size distribution and seasonal variation of atmospheric cellulose [J]. Atmospheric Environment, 2003, 37: 3693-3699. doi: 10.1016/S1352-2310(03)00451-5
[15] Sánchez-Ochoa A, Kasper-Giebl A, Puxbaum H, Gelencser A, Legrand M, Pio C.Concentration of atmospheric cellulose: A proxy for plant debris across a west-east transect over Europe[J].Journal of Geophysical Research,2007,112,D23S08. doi: 10.1029/2006jd008180.
[16] Cerqueira M, Marques D, Caseiro A, Pio C. Experi-mental evidence for a significant contribution of cellulose to indoor aerosol mass concentration [J].Atmospheric Environment, 2010, 44: 867-871. doi: 10.1016/j.atmosenv.2009.11.043
[17] Kunit M, Puxbaum H. Enzymatic determination of the cellulose content of atmospheric aerosols [J]. Atmospheric Environment, 1996, 30: 1233-1236. doi: 10.1016/1352-2310(95)00429-7
[18] Butler G W, Bailey R W. Chemistry and Biochemistry of Herbage (Volume Ⅰ) [M]. New York: Academic Press, 1973.
[19] 欧阳平凯,陈茺,陈育如.木质纤维素原料浓酸水解动力学研究[J].林产化学与工业, 1993, 13 (1): 77-82. http://www.cnki.com.cn/Article/CJFDTOTAL-LCHX199301013.htm
[20] 王林风,程远超.硝酸乙醇法测定纤维素含量[J].化学研究, 2011, 22(4): 52-55. http://www.cnki.com.cn/Article/CJFDTOTAL-HXYA201104015.htm
[21] Browning B L, Bublite I O. The isolation of holocell-ulose from wood [J].Tappi, 1953, 36(10): 452-458.
[22] Caserio A. Chemical Composition of the European Aerosol [D].Portugal: University of Aveiro, 2008.
[23] Zhang T, Claeys M, Cachier H, Dong S P, Wang W, Maenhaut W, Liu X D. Identification and estimation of the biomass burning contribution to Beijing aerosol using levoglucosan as a molecular marker [J]. Atmospheric Environment, 2008, 42: 7013-7021. doi: 10.1016/j.atmosenv.2008.04.050
[24] 胡敏.北京大气细粒子和超细粒子理化特征、来源及形成机制[M].北京:科学出版社, 2009.
-


 下载:
下载: